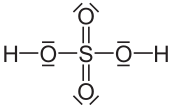
El ácido sulfúrico es un compuesto químico extremadamente corrosivo cuya fórmula es H2SO4. Es el compuesto químico que más se produce en el mundo, por eso se utiliza como uno de los tantos medidores de la capacidad industrial de los países. Una gran parte se emplea en la obtención de fertilizantes. También se usa para la síntesis de otros ácidos y sulfatos y en la industria petroquímica.
Generalmente se obtiene a partir de dióxido de azufre, por oxidación con óxidos de nitrógeno en disolución acuosa. Normalmente después se llevan a cabo procesos para conseguir una mayor concentración del ácido. Antiguamente se lo denominaba aceite o espíritu de vitriolo, porque se producía a partir de este mineral.
La molécula presenta una estructura piramidal, con el átomo de azufre en el centro y los cuatro átomos de oxígeno en los vértices. Los dos átomos de hidrógeno están unidos a los átomos de oxígeno no unidos por enlace doble al azufre. Dependiendo de la disolución, estos hidrógenos se pueden disociar. En agua se comporta como un ácido fuerte en su primera disociación, dando el anión hidrogenosulfato, y como un ácido débil en la segunda, dando el anión sulfato.
Tiene un gran efecto deshidratante sobre las moléculas hidrocarbonadas como la sacarosa. Esto quiere decir que es capaz de captar sus moléculas en forma de agua, dejando libre los átomos de carbono con la consiguiente formación de carbono puro.
ácido carbónico
El ácido carbónico es un ácido oxácido proveniente del dióxido de carbono (CO2), siendo su composición H2CO3.2 También es llamado dihidrogeno (trioxidocarbonato), trioxocarbonato (IV) de hidrógeno o ácido trioxocarbónico (IV). Es un ácido débil pues su constante de ionización es muy pequeña, Ka : 0,000 000 45.3El ácido carbónico puede atacar a muchos de los minerales que comúnmente forman las rocas calizas o margosas, descomponiéndolos por ejemplo en bicarbonato de calcio
Es el producto de la reacción de agua y óxido de carbono (IV) y existe en equilibrio con este último, por ejemplo, en el agua gasificada o la sangre. No es posible obtener ácido carbónico puro ya que la presencia de una sola molécula de agua catalizaría su descomposición inmediata en óxido de carbono (IV) y agua. Sin embargo, se calcula que en ausencia absoluta de agua sería estable.
En disolución, el ácido carbónico puede perder uno o dos protones. Retirando el primer protón forma el anión bicarbonato; retirando el segundo protón forma el anión carbonato.
- H2CO3 → HCO3- + H+ (pKd = 6,35)
- HCO3- → CO32- + H+ (pKd = 10,33)
ácido clorhídrico
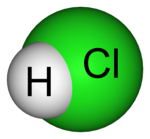
El ácido clorhídrico, ácido muriático, espíritu de sal, ácido marino, ácido de sal o todavía ocasionalmente llamado, ácido hidroclórico (traducción del inglés hydrochloric acid), agua fuerte o salfumán (en España), es una disolución acuosa del gas cloruro de hidrógeno (HCl). Es muy corrosivo y ácido. Se emplea comúnmente como reactivo químico y se trata de un ácido fuerte que se disocia completamente en disolución acuosa. Una disolución concentrada de ácido clorhídrico tiene un pH inferior a 1; una disolución de HCl 0,1 M da un pH de 1 (Con 40 mL es suficiente para matar a un ser humano, en un litro de agua. Al disminuir el pH provoca la muerte de todo el microbioma gastrointestinal, además de la destrucción de los tejidos gastrointestinales).
A temperatura ambiente, el cloruro de hidrógeno es un gas ligeramente amarillo, corrosivo, no inflamable, más pesado que el aire, de olor fuertemente irritante. Cuando se expone al aire, el cloruro de hidrógeno forma vapores corrosivos densos de color blanco. 4El cloruro de hidrógeno puede ser liberado por volcanes.
El cloruro de hidrógeno tiene numerosos usos. Se usa, por ejemplo, para limpiar, tratar y galvanizar metales, curtir cueros, y en la refinación y manufactura de una amplia variedad de productos.4 El cloruro de hidrógeno puede formarse durante la quema de muchos plásticos. Cuando entra en contacto con el agua, forma ácido clorhídrico. Tanto el cloruro de hidrógeno como el ácido clorhídrico son corrosivos.
Ácido acetilsalicílico
| Ácido acetilsalicílico | ||
|---|---|---|
 | ||
 | ||
| Nombre (IUPAC) sistemático | ||
| Ácido 2-(acetiloxi)-benzoico | ||
| Identificadores | ||
| Número CAS | 50-78-2 | |
| Código ATC | B01AC06 | |
| PubChem | 2244 | |
| DrugBank | APRD00264 | |
| ChEBI | 15365 | |
| Datos químicos | ||
| Fórmula | C9H8O4 | |
| Peso mol. | 180,16 g/mol | |
| Sinónimos | Ácido 2-etanoatobenzoico, Ácido acetilsalicílico, Ácido o-acetilsalicílico, Acetilsalicilato, Ácido 2-acetoxibenzoico | |
| Datos físicos | ||
| Densidad | 1,40 g/cm³ | |
| P. de fusión | 138 °C (280 °F) | |
| P. de ebullición | 140 °C (284 °F) | |
| Solubilidad en agua | 1 mg/mL (20 °C) | |
| Farmacocinética | ||
| Biodisponibilidad | Rápida y completa | |
| Unión proteica | 99,6 % | |
| Metabolismo | hepático | |
| Vida media | 300-650mg: 3,1-3,2 horas; Dosis 1 g:5 horas; Dosis 2 g:9 horas | |
| Excreción | Renal | |
| Datos clínicos | ||
| Cat. embarazo | C (AU) No hay estudios en humanos. El fármaco sólo deben utilizarse cuando los beneficios potenciales justifican los posibles riesgos para el feto. Queda a criterio del médico tratante. (EUA) | |
| Estado legal | Unscheduled (AU) OTC (Venta sin receta como monofármaco, combinación, o a dosis bajas)(MEX) GSL (UK) OTC (EUA) | |
| Vías de adm. | Oral | |
| [editar datos en Wikidata] | ||
El ácido acetilsalicílico o AAS (C9H8O4), conocido popularmente como aspirina, nombre de una marca que pasó al uso común, es un fármaco de la familia de los salicilatos. Se utiliza como medicamento para tratar el dolor (analgésico), la fiebre (antipirético) y la inflamación (antiinflamatorio), debido a su efecto inhibitorio, no selectivo, de la ciclooxigenasa.1 2
Se utiliza también para tratar inflamaciones específicas tales como la enfermedad de Kawasaki, la pericarditis o la fiebre reumática. La administración de aspirina poco después de un ataque al corazón disminuye el riesgo de muerte y su uso a largo plazo ayuda a prevenir ataques cardíacos,34 accidentes cerebrovasculares y coágulos de sangre en personas con alto nivel de riesgo.1 Puede disminuir el riesgo de padecer ciertos tipos de cáncer, en especial el cáncer colorrectal.5 En el tratamiento del dolor o la fiebre, sus efectos comienzan de forma típica a los treinta minutos.1 El ácido acetilsalicílico es el antiinflamatorio no esteroideo (AINE) por excelencia y funciona de forma similar a otros AINE, aunque bloquea el normal funcionamiento de las plaquetas1 (antiagregante plaquetario).6
Entre los efectos secundarios comunes se encuentra la dispepsia y entre los efectos secundarios más importantes la úlcera péptica, la perforación del estómago y el empeoramiento del asma. El riesgo de hemorragia aumenta en personas mayores, consumidores de alcohol, de otros antiinflamatorios no esteroideos o de anticoagulantes. La aspirina no está recomendada en mujeres que se encuentren en la última fase del embarazo. En general, tampoco está recomendada en niños con infecciones, debido al riesgo de sufrir el síndrome de Reye,7 y en dosis altas puede provocar tinnitus (zumbido en los oídos).
Ácido hialurónico
El ácido hialurónico (AH) es un polisacárido del tipo de glucosaminoglucanos con enlaces β, que presenta función estructural, como los sulfatos de condroitina. De textura viscosa, existe en la sinovia, humor vítreo y tejido conjuntivo colágeno de numerosos organismos y es un importante glucosoaminoglucano en la homeostasis articular.1 En seres humanos destaca su concentración en las articulaciones, los cartílagos y la piel. En un hombre medio de 70 kilogramos de peso puede haber una cantidad total de 15 gramos de ácido hialurónico en su cuerpo, y un tercio de éste se degrada y sintetiza cada día.2
Está constituido por cadenas de carbohidratos complejos, en concreto unos 50 000 disacáridos de N-acetilglucosamina y ácido glucurónico por molécula.3 y deriva de la unión de amino azúcares y ácidos urónicos. Esta cadena se sitúa formando espirales con un peso molecular medio de 2 a 4 millones. Presenta la propiedad de retener grandes cantidades de agua y de adoptar una conformación extendida en disolución, por lo que son útiles a la hora de acojinar o lubricar. Estas propiedades se consiguen gracias al gran número de grupos OH y de cargas negativas de esta molécula, lo que permite, por el establecimiento de fuerzas de repulsión, que se conserven relativamente separadas entre sí las cadenas de carbohidratos.
Ácido acético
| ácido acético | ||
|---|---|---|
 Estructura plana del ácido acético | ||
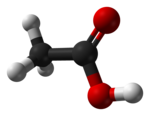 Estructura tridimensional del ácido acético | ||
| Nombre IUPAC | ||
| ácido etanoico | ||
| General | ||
| Otros nombres | Ácido acético | |
| Fórmula semidesarrollada | CH3COOH | |
| Fórmula molecular | C2H4O2 | |
| Identificadores | ||
| Número CAS | 64-19-71 | |
| Número RTECS | AF1225000 | |
| ChEBI | 15366 | |
| ChemSpider | 171 | |
| DrugBank | DB03166 | |
| PubChem | 176 | |
| UNII | Q40Q9N063P | |
| KEGG | D00010 | |
| Propiedades físicas | ||
| Apariencia | cristales | |
| Densidad | 1049 kg/m3; 1,049 g/cm3 | |
| Masa molar | 60,021129372 g/mol | |
| Punto de fusión | 290 K (17 °C) | |
| Punto de ebullición | 391,2 K (118 °C) | |
| Propiedades químicas | ||
| Acidez | 4,76 pKa | |
| Momento dipolar | 1,74 D | |
| Peligrosidad | ||
| SGA |   | |
| NFPA 704 | 
2
3
0
| |
| Frases R | R10, R35 | |
| Frases S | S1/2, S23, S26, S45 | |
| Riesgos | ||
| Ingestión | Dolor de garganta, vómito, diarrea, dolor abdominal, sensación de quemazón en el tracto digestivo. | |
| Inhalación | Dolor de garganta, dificultad respiratoria, tos. | |
| Piel | Irritación, graves quemaduras. | |
| Ojos | Irritación, visión borrosa, quemaduras profundas. | |
| Compuestos relacionados | ||
| Ácidos relacionados | Ácido metanoico Ácido propílico Ácido butírico | |
| Compuestos relacionados | Acetamida Acetato de etilo, Anhidrido acético, Acetonitrilo, Acetaldehído, Etanol, Cloruro de etanoilo | |
| Valores en el SI y en condiciones estándar (25 °C y 1 atm), salvo que se indique lo contrario. | ||
| [editar datos en Wikidata] | ||
El ácido acético (también llamado ácido metilcarboxílico o ácido etanoico) puede encontrarse en forma de ion acetato. Se encuentra en el vinagre, y es el principal responsable de su sabor y olor agrios. Su fórmula es CH3-COOH (C2H4O2). De acuerdo con la IUPAC, se denomina sistemáticamente ácido etanoico.
Es el segundo de los ácidos carboxílicos, después del ácido fórmico o metanoico, que solo tiene un carbono, y antes del ácido propanoico, que ya tiene una cadena de tres carbonos.
El punto de fusión es 16,6 °C y el punto de ebullición es 117,9 °C.
En disolución acuosa, puede perder el protón del grupo carboxilo para dar su base conjugada, el acetato. Su pKa es de 4,8 a 25 °C, lo cual significa, que al pH moderadamente ácido de 4,8, la mitad de sus moléculas se habrán desprendido del protón. Esto hace que sea un ácido débil y que, en concentraciones adecuadas, pueda formar disoluciones tampón con su base conjugada. La constante de disociación a 20 °C es Ka = 1,75·10−5.
Es de interés para la química orgánica como reactivo, para la química inorgánica como ligando, y para la bioquímica como metabolito (activado como acetil-coenzima A). También se utiliza como sustrato, en su forma activada, en reacciones catalizadas por las enzimas conocidas como acetiltransferasas y, en concreto, histona acetiltransferasas.
Hoy día, la vía natural de su obtención es a través de la carbonilación (reacción con CO) de metanol. Antaño se producía por oxidación de etileno en acetaldehído, el cual se oxidaba posteriormente para obtener, finalmente, el ácido acético.
Ácido cítrico
| Ácido cítrico | ||
|---|---|---|
 | ||
| Nombre IUPAC | ||
| Ácido 3-carboxi-3-hidroxi pentanodioico | ||
| General | ||
| Otros nombres | Ácido cítrico | |
| Fórmula estructural | 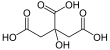 | |
| Fórmula molecular | C6H8O7 | |
| Identificadores | ||
| Número CAS | 77-92-91 | |
| Número RTECS | GE7350000 | |
| ChEBI | 41523 30769, 41523 | |
| ChemSpider | 305 | |
| DrugBank | 04272 | |
| PubChem | 311 | |
| Propiedades físicas | ||
| Densidad | 1665 kg/m3; 1,665 g/cm3 | |
| Masa molar | 192,13 g/mol | |
| Punto de fusión | 448 K (175 °C) | |
| Propiedades químicas | ||
| Acidez | 1=3,15; 2=4,77; 3=6,40 pKa | |
| Solubilidad en agua | 133 g/100 ml (22 °C) | |
| Riesgos | ||
| Riesgos principales | Irrita piel y ojos. | |
| Valores en el SI y en condiciones estándar (25 °C y 1 atm), salvo que se indique lo contrario. | ||
| [editar datos en Wikidata] | ||
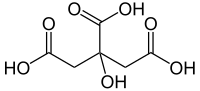
El ácido cítrico es un ácido orgánico tricarboxílico,2 presente en la mayoría de las frutas, sobre todo en cítricos como el limón y la naranja. Su fórmula molecular es C6H8O7.3
Es un buen conservante y antioxidante natural que se añade industrialmente como aditivo en el envasado de muchos alimentos como las conservas de vegetales enlatadas.
En bioquímica aparece como un metabolito intermediario en el ciclo de los ácidos tricarboxílicos, proceso realizado por la mayoría de los seres vivos.
El nombre IUPAC del ácido cítrico es ácido 2-hidroxi-1,2,3-propanotricarboxilico.4
Ácido ascórbico
| Ácido ascórbico | ||
|---|---|---|
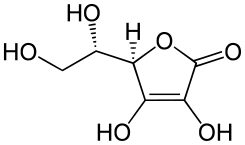 | ||
 | ||
| Nombre IUPAC | ||
| 5-((s)-1,2-dihidroxietil)-3,4-dihidroxifuran-2(5H)-ona | ||
| General | ||
| Otros nombres | Vitamina C | |
| Fórmula molecular | C 6H 8O 6 | |
| Identificadores | ||
| Número CAS | 50-81-71 | |
| ChEBI | 40892 | |
| PubChem | 5785 | |
| Propiedades físicas | ||
| Apariencia | polvo blanco | |
| Densidad | 1650 kg/m3; 1.65 g/cm3 | |
| Masa molar | 176.12 g/mol | |
| Punto de fusión | 463 K (190 °C) | |
| Propiedades químicas | ||
| Solubilidad en agua | 33 g/100 mL | |
| Valores en el SI y en condiciones estándar (25 °C y 1 atm), salvo que se indique lo contrario. | ||
| [editar datos en Wikidata] | ||
El ácido ascórbico es un cristal incoloro, inodoro, sólido, soluble en agua, con un sabor ácido. Es un ácido orgánico, con propiedades antioxidantes, proveniente del azúcar.
En humanos, primates y cobayas, entre otros, la vitamina C (enantiómero L del ácido ascórbico) no se sintetiza, por lo que debe ingerirse a través de los alimentos. Esto se debe a la ausencia de la enzima L-gluconolactona oxidasa, que participa en la ruta del ácido úrico.
Ácido fórmico
| Ácido fórmico | ||
|---|---|---|
 Estructura química | ||
 Estructura tridimensional | ||
| Nombre IUPAC | ||
| Ácido metanoico | ||
| General | ||
| Otros nombres | Ácido fórmico, ácido metanoico | |
| Fórmula semidesarrollada | H-COOH | |
| Fórmula estructural | Ver imagen | |
| Fórmula molecular | C H2O2 | |
| Identificadores | ||
| Número CAS | 64-18-61 | |
| Número RTECS | LQ4900000 | |
| ChEBI | 30751 | |
| ChemSpider | 278 | |
| DrugBank | 01942 | |
| PubChem | 284 | |
| Propiedades físicas | ||
| Apariencia | Incoloro | |
| Densidad | 1218.3 kg/m3; 1,2183 g/cm3 | |
| Masa molar | 46,03 g/mol | |
| Punto de fusión | 281,5 K (8 °C) | |
| Punto de ebullición | 373,8 K (101 °C) | |
| Viscosidad | 1,789 cP (20 °C) | |
| Propiedades químicas | ||
| Acidez | 3,74 pKa | |
| Solubilidad en agua | Soluble. | |
| Momento dipolar | 3,79 D | |
| Peligrosidad | ||
| Punto de inflamabilidad | 323 K (50 °C) | |
| NFPA 704 | 
2
3
1
COR
| |
| Temperatura de autoignición | 874 K (601 °C) | |
| Frases R | R10 R35 | |
| Frases S | S1/2 S23 S26 S45 | |
| Riesgos | ||
| Ingestión | Dolor de garganta, sensación de quemazón del tracto digestivo, dolor abdominal, diarrea, vómitos. | |
| Inhalación | Sensación de quemazón, tos, dificultad respiratoria, jadeo; síntomas de efectos no inmediatos. | |
| Piel | Enrojecimiento,dolor, quemaduras cutáneas graves. | |
| Ojos | Dolor, enrojecimiento, visión borrosa, quemaduras profundas graves. | |
| Compuestos relacionados | ||
| Ácidos relacionados | Ácido etanoico | |
| Otros compuestos relacionados | Metanal Metanol Metano | |
| Valores en el SI y en condiciones estándar (25 °C y 1 atm), salvo que se indique lo contrario. | ||
| [editar datos en Wikidata] | ||
El ácido metanoico, también llamado ácido fórmico, es un ácido orgánico de un solo átomo de carbono, y por lo tanto el más simple de los ácidos orgánicos. Su fórmula es H-COOH (CH2O2).


